аортокоронарное шунтирование и стентирование в чем разница
Информация для врачей
На наиболее часто задаваемые вопросы по теме сравнительной оценки результатов баллонной ангиопластики со стентированием и аорто-коронарного шунтирования отвечает Роберт Йонес ( Robert H. Jones), профессор Дюкского института клинических исследований, г.Дарем, Северная Каролина, США (Duke Clinical Research Institute, Durham, NC,USA).
1. Какие основные клинические показатели прогнозируют ближайшую смертность и определяют продолжительность жизни после установления диагноза ишемической болезни сердца?
Клиническими показателями, прогнозирующими высокую вероятность смерти в ближайшем периоде после установления диагноза ИБС, являются дисфункция левого желудочка, обширность поражения коронарных артерий, застойная сердечная недостаточность и острота ( скорость) развития симптомов. Кроме перечисленных, к таковым относятся пожилой возраст, наличие в анамнезе перенесенной кардиохирургической операции и патологии сосудов других бассейнов, а также сопутствующие заболевания, особенно почек и легких. Клиническими показателями, влияющими на продолжительность жизни, вне зависимости от вида выбранной терапии, также являются фракция выброса левого желудочка, возраст, сопутствующие заболевания, сосудистые заболевания других бассейнов, застойная сердечная недостаточность и инфаркт миокарда на протяжении 24 часов от момента возникновения.
2. Каково взаимодействие этих показателей с выбранным лечением, и какой показатель лучше всего распознает наиболее эффективное лечение у конкретного больного?
Достижение оптимальной стратегии выбора наиболее соответствующей конкретному больному терапии имело бы тенденцию уравнивать значение прогностических факторов в общей популяции больных и тем самым уничтожало бы различия между видами лечения, наблюдаемые при оценке отдельно взятого показателя. Если выбор лечения мог бы быть идеальным, роль каждого прогностического показателя сосредоточилась бы только на его биологическом значении. Большинство показателей, которые прогнозируют высокий риск медикаментозного лечения у пациентов с ИБС, также прогнозируют повышенный риск у пациентов, которым выполняется баллонная ангиопластика и аорто-коронарное шунтирование.
Анатомия коронарных артерий – единственное исключение из этого обобщения. Поэтому этот показатель наиболее полезен в определении самого эффективного вида лечения у конкретного пациента. Более обширное коронарное поражение или более значимая степень сужения артерий связаны с повышенной смертностью при медикаментозном ведении пациентов, в отличие от лишь минимального увеличения степени риска смерти при лечении хирургическим методом. Пациенты, подверженные баллонной ангиопластике со стентированием, имеют тенденцию находиться по результатам лечения в зависимости от обширности анатомического поражения коронарных сосудов между перенесшими АКШ и леченными медикаментами. Все другие прогностические факторы имеют тенденцию повышать относительный риск одинаково во всех группах с различными видами лечения.
Поэтому, какая-либо абсолютная выгода от любого интервенционного вида лечения, как производная коронарной анатомии, имеет тенденцию усиливаться другими предвестниками повышенного риска.
3. Какие характеристики коронарной анатомии лучше всего определяют прогноз, и какова взаимосвязь проводимого лечения и его результата как производной от обширности поражения коронарного русла?
Коронарная анатомия, имеющая связь с прогнозом и полезная с точки зрения оценки правильности выбранного вида лечения, включает 75% — 95%-ную степень сужения и локализацию этого сужения в передней межжелудочковой артерии. Пациентам с 60% или более сужением ствола левой коронарной артерии наиболее показана хирургия с точки зрения влияния на продолжительность жизни в сравнении с медикаментозным лечением или баллонной ангиопластикой, и эти пациенты должны получить именно хирургическое лечение. За исключением пациентов с 95% сужением проксимального сегмента передней межжелудочковой артерии, пациенты с поражением единственного коронарного сосуда, леченные только медикаментозно, имеют достаточно хороший прогноз, а дополнение лечения баллонной ангиопластикой или АКШ существенно не изменяет их продолжительность жизни. Интервенционная терапия у этих пациентов обычно используется для избавления от стенокардии или болевого синдрома вследствие острой коронарной окклюзии. Так как продолжительность жизни больных с поражением одной артерии ( за исключением выраженного сужения проксимального сегмента передней межжелудочковой артерии, прим.пер.) хорошее или даже лучше чем с АКШ, поражение, которое может быть подвергнуто баллонной ангиопластике, должно быть устранено именно этим типом лечения.
4. Каковы ранние результаты чрезкожной чрезпросветной коронарной ангиопластики (PTCA ) и аорто-коронарного шунтирования у пациентов с двух — и трехсосудистым поражением?
Девять рандомизированных ( т.е. при выборке больных использовался принцип – выбор наобум, прим.пер.) исследований были проведены для определения пользы баллонной ангиопластики в сравнении с АКШ в популяции 5,200 пациентов, имеющих поражение двух или трех коронарных сосудов. Индивидуальные и групповые результаты не показали различий в плане выживания, но эти результаты полезны в индивидуализации лечения у определенных пациентов с двумя или тремя пораженными коронарными сосудами. Самым большим из этих исследований был исследовательский проект BARY (Bypass Angioplasty Revascularization Investigation), проводимый 18-тью Североамериканскими центрами с рандомизацией 1828 пациентов с двумя или тремя пораженными сосудами, которые получали лечение баллонной дилатацией или АКШ между 1988 и 1991 годами. Таблица демонстрирует, что « внутрибольничный» исход двух интервенционных методов лечения ИБС не отличался друг от друга.
Исходы методов « в больнице»
Что выбрать коронарное шунтирование или стентирование?
В сентябрьском номере журнала «The American Journal of Cardiology» опубликованы результаты ретроспективного исследования, оценивающего влияние фракции выброса левого желудочка (ФВ ЛЖ) на долговременные исходы после разных методов реваскуляризации миокарда.
Анализ выполнен на основании выборки из базы данных «CREDO-Kyoto PCI/CABG Registry Cohort-2», в исследование включено 3584 пациентов с 3-сосудистым поражением и/или поражением ствола левой коронарной артерии, которым реваскуляризация миокарда выполнена впервые. У 2676 пациентов из них зарегистрированы нормальные показатели ФВ ЛЖ ( >50%) и 908 с ФВ ЛЖ ≤50%.
Среди пациентов с нормальной ФВ ЛЖ смертность от всех причин и смертность от ССЗ статистически значимо не отличалась в группах после коронарного шунтирования (КШ) и после рентгенэндоваскулярных методов (стентирование, ангиопластика) реваскуляризации миокарда.
Среди пациентов с ФВ ЛЖ ≤50% риск смерти в отдаленный период был значительно выше после рентгенэндоваскулярных методов реваскуляризации миокарда, чем после КШ. Отношение рисков составило 1.49, 95% ДИ 1.04 — 2.14, p = 0.03 для смерти от всех причин и 2.39, 95% ДИ 1.43 — 3.98, p 35%, но ≤ 50% отношение рисков смерти от всех причин составило 2.25, 95% ДИ 1.15 — 4.40, p = 0.02 и 4.42 для смерти от ССЗ, 95% ДИ 1.48 13.24, p = 0.01.
Источник Am J Cardiol. 2014 Jul 16. pii: S0002-9149(14)01433-7. Comparison of Five-Year Outcomes of Coronary Artery Bypass Grafting Versus Percutaneous Coronary Intervention in Patients With Left Ventricular Ejection Fractions ≤50% Versus >50% (from the CREDO-Kyoto PCI/CABG Registry Cohort-2). Marui A1, Kimura T2, Nishiwaki N3, Mitsudo K4, Komiya T5, Hanyu M6, Shiomi H2, Tanaka S7, Sakata R8; The CREDO-Kyoto PCI/CABG Registry Cohort-2 Investigators.
Комментарий: уже более 10 лет регулярно обновляются клинические рекомендации, отражающие принципы выбора метода реваскуляризации в определенных ситуациях. Практически неизменной остается рекомендация о предпочтении выполнения КШ пациентам с хроническими стабильными формами ИБС при 3-хсосудистом поражении и поражением ствола левой коронарной артерии, особенно при снижении ФВ ЛЖ. Однако, в реальной практике среди пациентов с такими характеристиками наиболее часто в дооперационный период регистрируется высокий риск периоперационной смерти и осложнений значимых для дальнейшего качества жизни пациентов. Поэтому и врачи, и пациенты очень часто стоят между Сциллой и Харибной. Что выбрать КШ с большим риском периоперационных осложнений, но вероятностью лучшего исхода в будущем или выбрать стентирование с меньшим риском осложнений и смерти во время выполнения вмешательства, но более высоким риском худшего прогноза в будущем? Вероятно, оптимальным сегодня является индивидуализированный подход, учитывающий результаты исследования, возможности и (что очень важно) периоперационные результаты применения разных методов реваскуляризации в конкретной клинике, а также мнение пациента.
Информация для пациентов
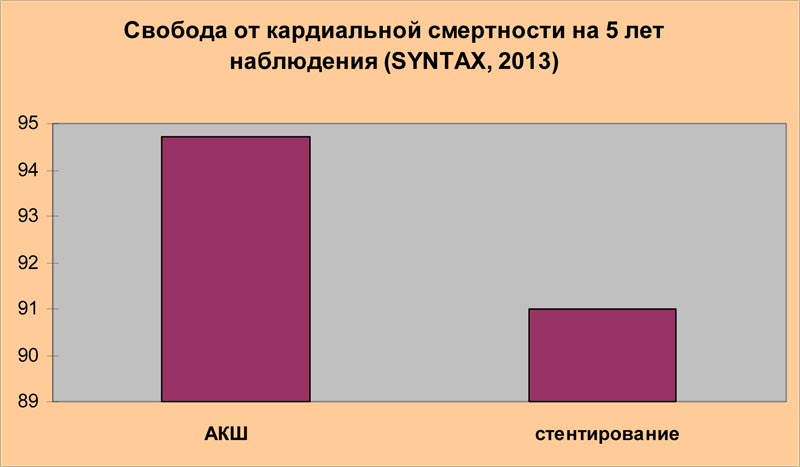
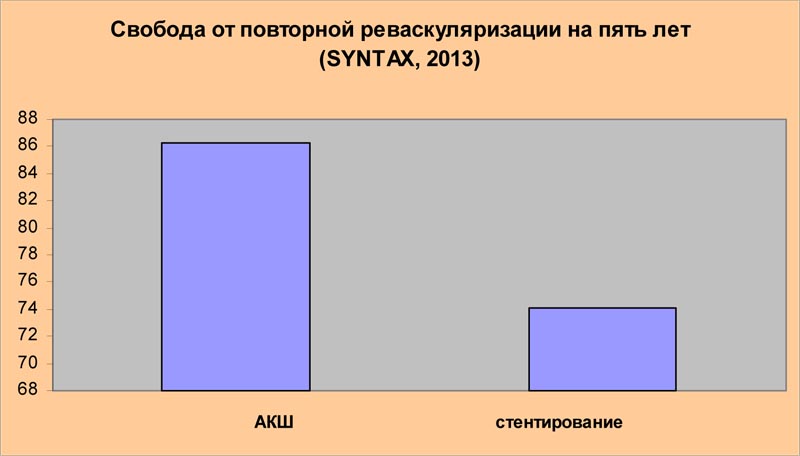
« Финальные пятилетние результаты исследования SYNTAX не только подтверждают, что аортокоронарное шунтирование ( АКШ) в сравнении со стентированием сопровождается более низкой частотой повторной реваскуляризации, но также демонстрируют значительную роль АКШ в снижении кардиальной смертности»
Цитата из доклада Piroze Davierwala and Friedrich W Mohr
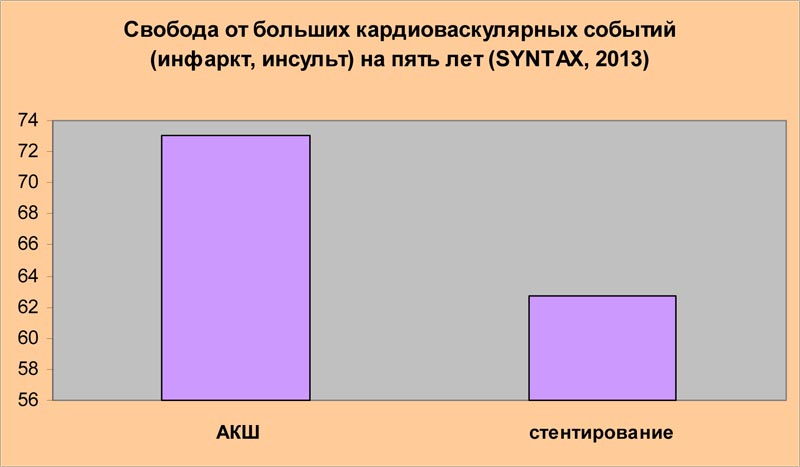
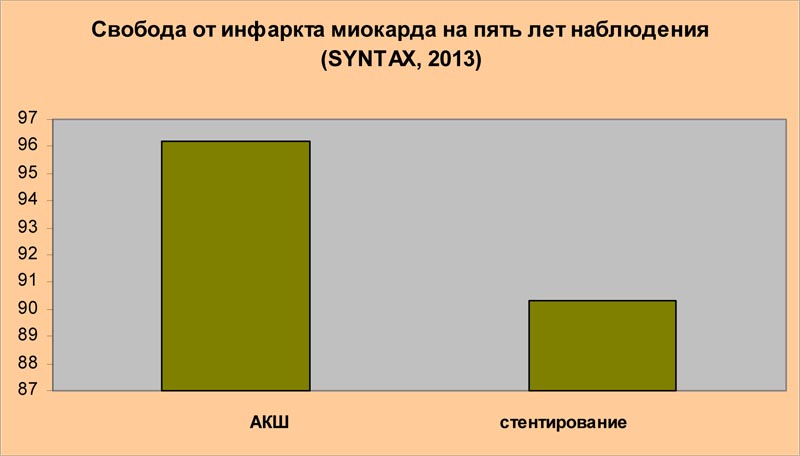
Доклад исследователей, проводивших рандомизированное проспективное испытание SYNTAX и обнаруживших неоспоримые преимущества аортокоронарного шунтирования по сравнению со стентированием по многим оцениваемым параметрам, казалось бы, должен стать жирной точкой в установлении истины и иметь результатом существенное ограничение использования стентов у плановых больных с множественным сужением коронарных артерий. Ниже приведены выдержки из сообщения авторов исследования SYNTAX, прозвучавшего в рамках 27-ой Ежегодной Встречи Европейской ассоциации кардиоторакальных хирургов в Вене, в октябре 2013 года:
Если суммировать данные, полученные в исследовании SYNTAX, то можно сделать вывод: для 63% всех пациентов остается статистически достоверно лучшим лечение с помощью АКШ; это включает пациентов АКШ регистра (644 человека); пациентов рандомизированного испытания ( с поражением главного ствола и трех артерий со значением по шкале SYNTAX ≥33 [605 пациентов], пациентов с тремя пораженными сосудами со значением по шкале SYNTAX ≤ 22 [574 пациентов], пациентов с поражением главного ствола и количеством баллов по шкале SYNTAX 23-32 [195 пациентов]).
К сожалению, вопреки очевидности и убедительности доказательной базы, стентирование продолжает своё « победоносное» шествие в лечении любых форм ИБС, в том числе и вне состояний острого нарушения коронарного кровообращения. Это шествие не ограничивает ничто, ни авторитетнейшие европейские или североамериканские руководящие принципы по восстановлению кровообращения сердца, ни статистически безукоризненные сравнительные испытания типа представленного выше исследования SYNTAX. Причем натиск стентирования является труднопреодолимым не только в нашей стране, где явления « противостояния очевидности» являются повсеместными, но и в упорядоченных странах Старого и Нового Света. Западные хирурги проявляют озабоченность в этом отношении. Приводим пример двух коротких публикаций в профессиональных журналах США.
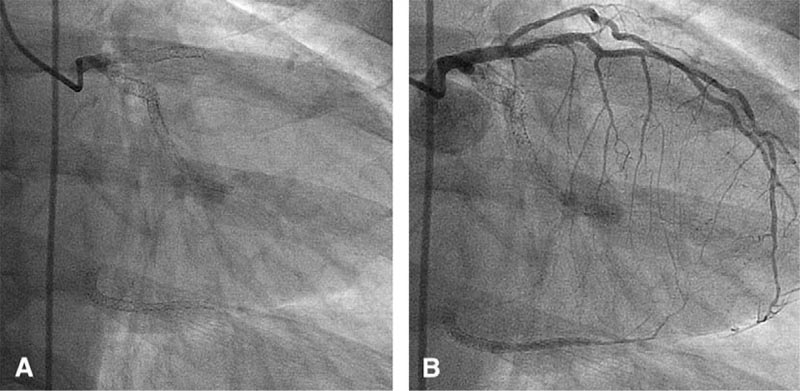
Рисунок 1. Множественные стенты в передней межжелудочковой артерии ( ПМЖВ), ветви тупого края и терминальной ветви огибающей артерии (A ), со значительными сужениями внутри стентов в ПМЖВ и полной внутристентовой окклюзией в ветви тупого края и терминальной ветви огибающей артерии (B ).
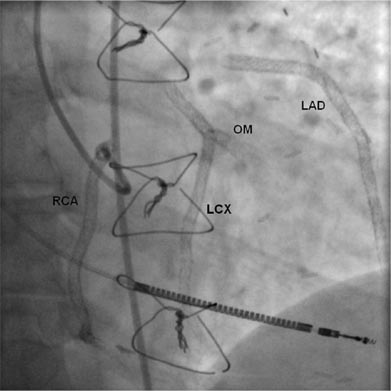
Рисунок 2. LAD – передняя межжелудочковая артерия; ОМ – ветвь тупого края; LCX – огибающая артерия; RCA – правая коронарная артерия
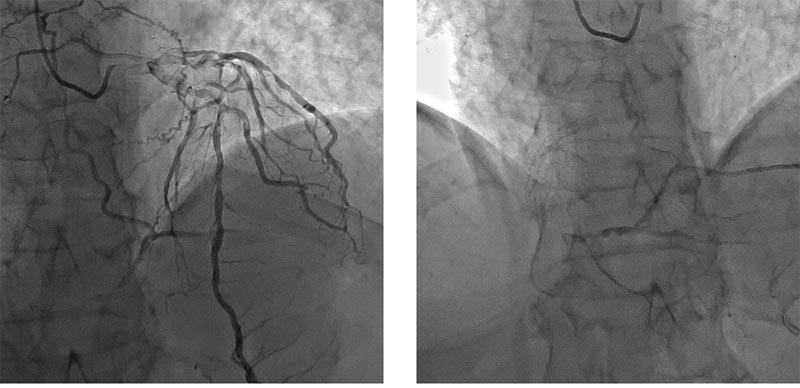
Представляем случай из нашей практики, который имеет несколько иное содержание, но в целом также характеризует ситуацию с выбором лечения плановой коронарной болезни сердца. Пациент 56 лет, имеет поражение всех коронарных сосудов, причем несколько стенозов локализуются в периферических сегментах артерий. Ангиографическая картина дает все основания предлагать пациенту аортокоронарное шунтирование. Однако неинформированный выбор больного склонился в пользу планового стентирования ( Рисунок 3).
Рисунок 3. В проксимальных отделах артерий видны тени стентов, одновременно контрастированные периферические части артерий демонстрируют грубые сужения или полное закрытие сосудов.
Вместо направления больного к кардиохирургу, пациенту в разных больницах была внедрена серия стентов в проксимальные сегменты артерий. При этом все периферические стенозы остались нетронутыми! В итоге, быстрое закрытие стента в правой коронарной артерии привело к её полной закупорке.
К сожалению, таких примеров множество! Неполная реваскуляризация ( состояние, когда не все артерии подвергаются восстановлению), восстановление проходимости сосуда, который не является причинным в развитии нарушения кровообращения у конкретного пациента, недостигнутая на всем протяжении ликвидация сужения являются частыми характеристиками стентирующих процедур у пациентов, с которыми нам приходится встречаться. И практически каждый такой случай сопровождается полным незнанием больным собственных перспектив, возможных сценариев течения заболевания, не говоря о необходимости встречи с кардиохирургом.
Каковы причины столь широкого, необоснованного, противоречащего фактам и доказательствам применения стентирования и снижения количества выполняемого АКШ? Попытаемся ответить на этот вопрос. В первую очередь, самым сильным аргументом в пользу стентирования является отсутствие необходимости в проведении полноценной хирургической операции. Это аргумент непреодолимой силы! Это аргумент аргументов, который заставляет пациента желать применения по отношению к нему только стентирования. Избегание хирургии – мощный маркетинговый спрос, который не ожидает, а жаждет предложений для своей реализации.
Конечно, чаяния пациентов избежать хирургии и бизнес-активность производителей стентов не являются единственными причинами выполнения стентирования вопреки рекомендациям и результатам сравнения с АКШ. Роль врачей кардиологов, впервые встречающихся с больным ишемической болезнью сердца, трудно переоценить. Именно от них исходит дуалистическая идеология равенства всех методов восстановления кровообращения сердца, будь то стентирование или АКШ. Мало того, многие кардиологи считают неудовлетворительными результаты всех интервенционных и хирургических методов, отдавая предпочтение медикаментозному лечению ИБС в плановых условиях и полагая, что фармацевтические компании генерируют всё новые и новые возможности в поддержку такой позиции. До сих пор среди кардиологов является распространенным тезис об улучшении качества жизни после АКШ при отсутствии увеличения её продолжительности. Данный тезис имеет неясный источник, и многократно опровергнут не только представленным исследованием SYNTAX, но и многими другими, проведенными ранее. В этих условиях, условиях отсутствия правдивой информации, выбор пациента удивления не вызывает.
Как это не покажется странным, но определенную отрицательную роль в формировании обсуждаемых уклонов сыграла организация медицинской помощи при остром коронарном синдроме. Именно в этих условиях применение стентирования является спасительным и неоспариваемым никакими сравнительными исследованиями. В приведенных выше клинических случаях пациенты поступали в больницы с острым расстройством коронарного кровообращения, получали стенты, состояние их улучшалось, и они проживали некоторое время до следующего острого коронарного синдрома, в лечении которого также применялись стенты и т.д., и т.д. В итоге, годы шли, количество стентов увеличивалось, побивало все рекорды, а контакт пациентов с кардиохирургами так и не состоялся. Необходимо осознавать, что выполненное стентирование по поводу острого коронарного синдрома не является полным и окончательным излечением, это тушение вспыхнувшего « пожара», угрожающего жизни. Ни пациент, ни его лечащий врач не должны считать излечение долгосрочным, а дальнейшую жизнь больного безоблачной. Это только полдороги к излечению, указание на необходимость контакта с кардиохирургом, который определит потребность в проведении АКШ для долгосрочного излечения. В связи с этим, необходимо информировать пациентов, попавших с острым коронарным синдромом в больницы, об обязательности осуществления записи визуальных данных коронарографии на компьютерные диски с последующей возможностью продемонстрировать их кардиохирургу. Запись коронарографии на диск обязательна еще и потому, что ценнейшая персональная информация о пациенте, которая может потребоваться в его дальнейшей жизни, будет утеряна безвозвратно!
Наконец, есть еще одна виноватая сторона – это мы, хирурги. Отсутствие какой-либо просветительской деятельности, недостаточная активность в отслеживании результатов своего труда, изолированность друг от друга и кардиологических служб – вот те составляющие, которые являются причиной необоснованного, неоправданного, бездоказательного и вредоносного для здоровья пациентов уклона лечения коронарной болезни сердца в сторону отказа от АКШ и необдуманного расширения выполнения внутрикоронарных вмешательств.
Цель настоящей статьи – частичное восполнение образовавшейся информационной бреши, призванное напомнить как самим себе, врачам, так и пациентам, имеющим коронарное поражение, о широких возможностях аортокоронарного шунтирования в лечении ИБС, существенно превышающих возможности внутрикоронарного стентирования.
1. J Am Coll Cardiol. 2005 Aug 16;46 (4 ):575-81. Five-year outcomes after coronary stenting versus bypass surgery for the treatment of multivessel disease: the final analysis of the Arterial Revascularization Therapies Study (ARTS ) randomized trial.
Serruys PW, Ong AT, van Herwerden LA, Sousa JE, Jatene A, Bonnier JJ, Schönberger JP, Buller N, Bonser R, Disco C, Backx B, Hugenholtz PG, Firth BG, Unger F.
2. Circulation. 2007 Mar 6;115 (9 ):1082-9. Five-year follow-up of the Medicine, Angioplasty, or Surgery Study (MASS II): a randomized controlled clinical trial of 3 therapeutic strategies for multivessel coronary artery disease.
Hueb W, Lopes NH, Gersh BJ, Soares P, Machado LA, Jatene FB, Oliveira SA, Ramires JA.
3. Circulation. 2008 Jul 22;118 (4 ):381-8. doi: 10.1161/CIRCULATIONAHA.107.739144. Epub 2008 Jul 7. Randomized, controlled trial of coronary artery bypass surgery versus percutaneous coronary intervention in patients with multivessel coronary artery disease: six-year follow-up from the Stent or Surgery Trial (SoS ).
Booth J, Clayton T, Pepper J, Nugara F, Flather M, Sigwart U, Stables RH; SoS Investigators.
4. Am Heart J. 2006 Jun;151 (6 ):1194-204. The SYNergy between percutaneous coronary intervention with TAXus and cardiac surgery (SYNTAX ) study: design, rationale, and run-in phase.
Ong AT, Serruys PW, Mohr FW, Morice MC, Kappetein AP, Holmes DR Jr, Mack MJ, van den Brand M, Morel MA, van Es GA, Kleijne J, Koglin J, Russell ME.
5. Lancet. 2013 Feb 23;381 (9867 ):629-38. doi: 10.1016/S0140-6736 (13 )60141-5.
Coronary artery bypass graft surgery versus percutaneous coronary intervention in patients with three-vessel disease and left main coronary disease: 5-year follow-up of the randomised, clinical SYNTAX trial. Mohr FW, Morice MC, Kappetein AP, Feldman TE, Ståhle E, Colombo A, Mack MJ, Holmes DR Jr, Morel MA, Van Dyck N, Houle VM, Dawkins KD, Serruys PW.
6. N Engl J Med. 2009 Mar 5;360 (10 ):961-72. doi: 10.1056/NEJMoa0804626. Epub 2009 Feb 18. Percutaneous coronary intervention versus coronary-artery bypass grafting for severe coronary artery disease. Serruys PW, Morice MC, Kappetein AP, Colombo A, Holmes DR, Mack MJ, Ståhle E, Feldman TE, van den Brand M, Bass EJ, Van Dyck N, Leadley K, Dawkins KD, Mohr FW; SYNTAX Investigators.
7. Eur J Cardiothorac Surg. 2010 Sep;38 Suppl:S1-S52. doi: 10.1016/j.ejcts.2010.08.019.
Guidelines on myocardial revascularization. Task Force on Myocardial Revascularization of the European Society of Cardiology (ESC ) and the European Association for Cardio-Thoracic Surgery (EACTS ); European Association for Percutaneous Cardiovascular Interventions (EAPCI ), Kolh P, Wijns W, Danchin N, Di Mario C, Falk V, Folliguet T, Garg S, Huber K, James S, Knuuti J, Lopez-Sendon J, Marco J, Menicanti L, Ostojic M, Piepoli MF, Pirlet C, Pomar JL, Reifart N, Ribichini FL, Schalij MJ, Sergeant P, Serruys PW, Silber S, Sousa Uva M, Taggart D.
8. The Journal of Thoracic and Cardiovascular Surgery, Volume 137, Number 4, p.1020-1021. Coronary stent disease: When will enough be enough? Igor E. Konstantinov, MD, PhD, Pankaj Saxena, MCh, DNB, and Jaffar Shehatha.
Ангиопластика и стентирование коронарных артерий
Ангиопластика коронарных артерий является методом лечения, который спасает тысячи жизней у пациентов с острым инфарктом миокарда. Появление этой технологии позволило снизить летальность при инфаркте в 10 раз и улучшить качество жизни у большинства пациентов с патологией коронарных артерий.
Отдаленные результаты коронарной ангиопластики и стентирования зависят от динамического наблюдения и используемых стентов. Современные стенты значительно улучшают прогноз дальнейшего течения заболевания.
В эндоваскулярной клинике Инновационного сосудистого центра достигнуты отличные результаты экстренных и плановых операций при ишемической болезни сердца. Для коррекции стенозов и окклюзий коронарных артерий у нас применяются самые современные эндоваскулярные инструменты (баллоны и стенты). Ежемесячно в клинике выполняются около 100 вмешательств на коронарных артериях у больных с острым коронарным синдромом и плановой стенокардией.
 Подготовка к коронарографии
Подготовка к коронарографии
Для планирования операции необходимо получить информацию о состоянии коронарных артерий и функции сердца. Для этого проводятся диагностические тесты, которые в экстренном случае включают в себя ЭКГ и лабораторную диагностику, а в плановом случае необходимо более детальное обследование.
Обследование перед плановой операцией включает в себя:
Перед операцией вам могут дать нагрузочную дозу антитромботических препаратов, чтобы избежать ранних тромботических осложнений.
Обезболивание и поддержка во время операции
Коронарная ангиопластика проводится без разрезов, поэтому не требует общего обезболивания. Достаточно местной анестезии места прокола артерии. С целью контроля за жизненно-важными функциями используется следящая аппаратура. Каждому пациенту подключается монитор, отображающий артериальное давление, ЭКГ и насыщение крови кислородом. Операция проводится под наблюдением анестезиолога-реаниматолога.
 Как проходит коронарная ангиопластика и стентирование
Как проходит коронарная ангиопластика и стентирование
Внутрь артерии проводится тонкий проводник, который идет до коронарных сосудов и должен преодолеть закупорку. Вместе с ним к сердцу проводится катетер, через который вводится контрастное вещество для ориентирования внутри сосуда. Выполняется серия коронарограмм и уточняется место закупорки артерий.Для выполнения ангиопластики проводник необходимо провести за место закупорки коронарной артерии. После проведения приступаем к самой процедуре ангиопластики.
Для этого по проводнику проводится специальный баллон в свернутом состоянии и устанавливается в месте сужения. С помощью специального устройства этот баллон раздувается и раскрывает просвет артерии. Процедура длится несколько секунд, чтобы не вызвать резкой боли в груди из-за блокирования кровотока в коронарной артерии.
Стент находится в артерии постоянно и со временем может зарастать, поэтому желательно использовать стенты покрытые лекарством, которые зарастают значительно медленнее и служат намного дольше.
В нашей клинике с успехом используется рассасывающийся стент Absorb, который сделан из материала, подвергающегося самораспаду с течением времени. При использовании такого стента через 2 года в коронарной артерии уже не остается инородного тела. Использование Absorb позволяет значительно улучшить отдаленные результаты коронарного стентирования.
После стентирования хирург проводит контрольное ангиографическое исследование убедившись в хорошем результате удаляет весь инструмент. На место доступа накладывается давящая повязка или используется специальное устройство для закрытия прокола.
Возможные риски при коронарной ангиопластике
Хотя ангиопластика является менее инвазивным способом, чем шунтирование это процедура по-прежнему сопряжена с некоторыми рисками. Риски могут быть связаны с самой процедурой и ее отдаленными исходами.
Ранние риски:
Поздние осложнения
 Прогноз после лечения
Прогноз после лечения
Коронарная ангиопластика значительно увеличивает поток крови через ранее суженную или закупоренную коронарную артерию. При этом боль в груди (стенокардия) обычно должна уменьшится, а физические возможности организма наоборот должны возрастать.
Нужно понимать, что ангиопластика и стентирование не излечивает ишемическую болезнь сердца, а лишь устраняет конкретные нарушения кровобращения сердечной мышцы. Для достижения стабильного результата необходимо вести здоровый образ жизни и принимать лекарства, предписанные врачом.
Если симптомы стенокардии возвращаются, то необходимо еще раз обратиться к своему врачу, а если появились боли в груди в покое, которые не реагируют на нитроглицерин, то вызывайте скорую помощь.
После коронарной ангиопластики и стентирования качество жизни улучшается у 95% пациентов, при этом у многих из них эффект сохраняется более 5 лет.
Послеоперационное наблюдение и лечение
Если проводится плановая операция, то срок госпитализации будет скорее всего не больше 2-х суток. После выполнения контрольной диагностики назначаются препараты и пациент выписывается домой. На работу можно выходить спустя неделю после операции. Однако, если операция проводилась по поводу инфаркта, то лечение будет продолжено примерно около месяца.
Немедленно свяжитесь с врачом в следующих случаях:
Необходимо проявлять внимательность в выполнении назначений врача и никогда самостоятельно не отменять назначенные препараты.
Чтобы сохранить сердце здоровым после ангиопластики необходимо:
 Подготовка к коронарографии
Подготовка к коронарографии Как проходит коронарная ангиопластика и стентирование
Как проходит коронарная ангиопластика и стентирование Прогноз после лечения
Прогноз после лечения