неполная инволюция тимуса на кт что это значит
Неполная инволюция тимуса на кт что это значит
Тимус является одним из основных органов лимфатической системы, играющим ключевую роль как в клеточном, так и в гуморальном иммунитете. Данный орган развивается из вентральной части глоточного кармана, покрыт капсулой и состоит из двух долей, расположенных в непосредственной близости от верхнего края перикарда, проксимальных отделов восходящей аорты и легочного ствола. Однако ткань тимуса может выявляться в любом месте на протяжении от шеи до реберно-диафрагмального угла.
Тимус имеет форму пирамиды с широким основанием внизу и двумя узкими рогами вверху. Несмотря на то что тимус активно функционирует на протяжении всей жизни, с возрастом наблюдается его жировая инволюция. У взрослых тимус при рентгенографии в норме не визуализируется, однако у лиц моложе 40 лет его можно увидеть при КТ или МРТ. После 40 лет по причине завершения жировой инволюции ткань тимуса обнаруживают редко.
а) Опухоли тимуса. Согласно классификации Всемирной организации здравоохранения (ВОЗ) опухоли, развивающиеся в тимусе или в переднем средостении вблизи тимуса, делят на эпителиальные новообразования (тимома, карцинома тимуса и карциноид тимуса), герминативноклеточные новообразования, медиастинальную лимфому (может поражать тимус), мезенхимальные новообразования (тимолипома, липома, липосаркома), эктопические новообразования (происходят из щитовидной или паращитовидной железы) и метастазы. Гистологическая классификация тимом, разработанная ВОЗ, широко используется в патологической анатомии, но в клинической практике ее применение затруднено из-за расхождений между специалистами по интерпретации полученных результатов, гистологической гетерогенности данного типа опухолей и слабой корреляции с клиническим исходом.
Однако следует отметить, что во многих опубликованных статьях тимомы согласно гистологической классификации ВОЗ подразделяют на опухоли с низким риском (типы А, АВ и В1) и опухоли с высоким риском (типы В2 и ВЗ).
Новообразования тимуса встречаются редко и составляют менее 1 % от всех злокачественных опухолей у взрослых. Вследствие этого опухоли тимуса изучены плохо, и публикации на эту тему, как правило, ограничиваются одноцентровыми ретроспективными обзорами, охватывающими большой промежуток времени. В 2010 году для «обеспечения строгих требований к структуре, организации и научности» исследований, посвященных злокачественным опухолям тимуса и средостения, была организована Международная группа по изучению злокачественных новообразований тимуса (ITMIG).
ITMIG представляет собой мультидисциплинарную группу экспертов (в том числе врачей лучевой диагностики), признанную Международным союзом по борьбе с раком (UICC) и Американским объединенным комитетом по изучению рака (AJCC).
Для стадирования множества злокачественных новообразований были разработаны классификации TNM, учитывающие распространенность первичной опухоли (Т), наличие метастазов в регионарных лимфатических узлах (N) и отдаленных метастазов (М). Однако стадирование эпителиальных опухолей тимуса обычно проводится согласно классификации Масаока-Кога. В настоящее время ITMIG работает над тем, чтобы создать в сотрудничестве с Международной ассоциацией по изучению рака легких (IASLC) классификацию TNM для стадирования злокачественных опухолей тимуса. Рассматривается возможность включения такой классификации в 8-е издание системы TNM, разрабатываемой AJCC/UICC.
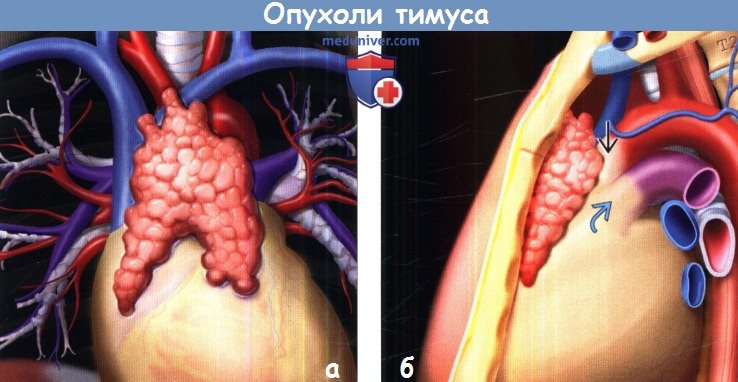
(б) На рисунке изображено положение тимуса в норме. Тимус локализуется в преваскулярном средостении и прилежит к начальным отделам легочного ствола и восходящей аорты.
б) Лучевая диагностика опухолей тимуса. Новообразования тимуса могут быть выявлены случайно вследствие обнаружения патологических изменений при отсутствии соответствующих симптомов, к которым относят паратимический синдром, связанный с неоплазией тимуса (например, при миастении, множественной эндокринной неоплазии), и симптомы, обусловленные объемным воздействием опухоли или ее местнодеструирующим ростом. Знание нормальной лучевой анатомии средостения и тимуса имеет большое значение для дифференцирования опухолевых образований тимуса с неопухолевыми. Диффузное увеличение тимуса может наблюдаться при его гиперплазии или лимфоматозном поражении. Изолированное объемное образование с большей вероятностью соответствует первичной злокачественной опухоли тимуса, часто — эпителиальной.
1. Рентгенография. Рентгенография органов грудной клетки является первичным методом диагностики, при котором можно выявить патологические изменения в тимусе. Заподозрить наличие патологического образования можно по изменению медиастинальных линий и полос, в том числе по утолщению передней соединительной линии, и по изменению контуров средостения, однако изменения могут быть выражены слабо. Вследствие внелегочной локализации патологические образования тимуса могут характеризоваться наличием симптома неполного контура и не визуализироваться при исследовании во взаимно перпендикулярных проекциях. Кроме того, небольшие патологические образования, расположенные по срединной линии, в прямой проекции могут не выходить за контур средостения.
При распространенных опухолях и опухолях с местнодеструирующим ростом могут обнаруживаться неровный их контур, высокое стояние купола диафрагмы вследствие инвазии диафрагмального нерва и «падающие» метастазы в плевре.
2. КТ. КТ с контрастным усилением является методом выбора для диагностики опухолей тимуса.
Такие опухоли обычно возникают у взрослых лиц, у которых тимус подвергается жировой инволюции. Поэтому мягкотканные опухоли тимуса хорошо визуализируются на фоне жировой ткани. Использование контрастного вещества позволяет выявлять признаки инвазивного роста новообразований: инфильтрацию жировой клетчатки средостения, исчезновение кпетчаточных пространств между патологическим образованием и прилежащими структурами, циркулярный охват или инвазию легких или сердца и сосудов, лимфаденопатию, сопутствующий плевральный или перикардиальный выпот и мягкотканные узелки и объемные образования.
КТ позволяет осуществлять предоперационное стадирование эпителиальных опухолей тимуса (особенно тимомы) и определять тактику лечения пациентов: выполнять хирургическое вмешательство, проводить неоадъювантную терапию при местно-распространенных опухолях или паллиативную химиотерапию при наличии лимфогенных и гематогенных метастазов. Крометого, КТ предпочтительнее использовать для оценки состояния пациентов со злокачественным новообразованием тимуса после проведенного лечения.
3. МРТ. МРТ также используется для выявления патологических изменений в тимусе и позволяет дифференцировать гиперплазию с неоплазией, поскольку первая характеризуется выраженным снижением интенсивности сигнала в противофазе. Кроме того, с помощью МРТ можно дифференцировать кистозные образования тимуса: в стенках кистозных опухолей в отличие от кист могут выявляться узелки. Также МРТ можно применять у тех пациентов, кому противопоказано вводить йодсодержащее контрастное вещество, что позволяет оценивать сосуды на предмет наличия инвазии даже без проведения контрастного усиления.
4. ФДГ-ПЭТ/КТ. ФДГ-ПЭТ/КТ не позволяет с точностью дифференцировать гиперплазию тимуса и неоплазию или так называемые тимомы с низким риском и тимомы с высоким риском. Однако данный метод используется для оценки злокачественных опухолей тимуса (например, карциномы) и обнаружения отдаленных метастазов и метастазов в лимфатических узлах.
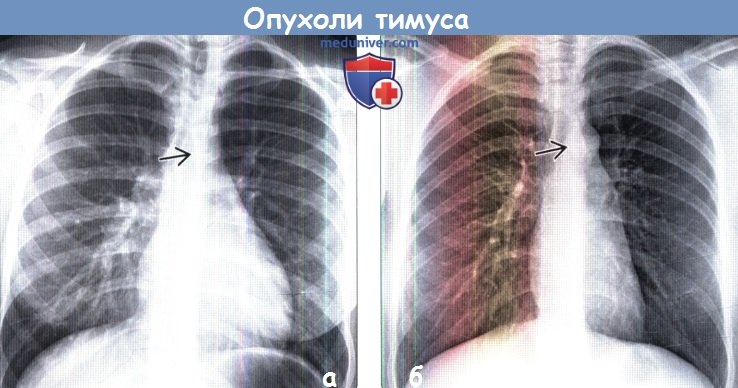
(б) Женщина 27 лет с диффузным токсическим зобом. При рентгенографии органов грудной клетки в ПП проекции визуализируется незначительное утолщение передней соединительной линии вследствие увеличения тимуса, вызванного его гиперплазией. При рентгенографии объемные образования тимуса могут проявляться слабо выраженными патологическими изменениями. 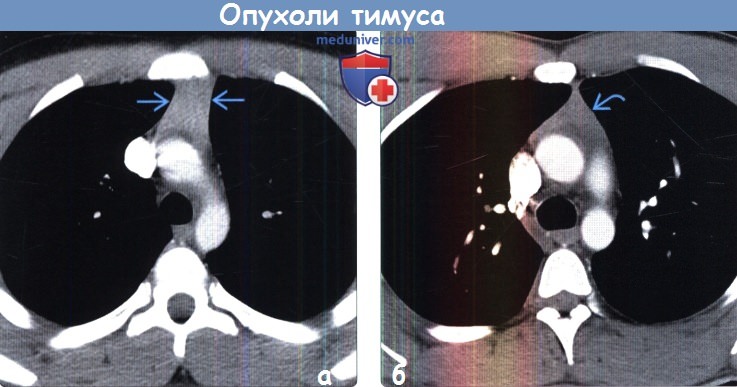
(б) У мужчины 21 года при КТ с контрастным усилением в преваскулярном отделе средостения визуализируется нормальный тимус, характеризующийся треугольной формой, гомогенной структурой и мягкотканной плотностью. Это нормальная лучевая картина для данного возраста.
Редактор: Искандер Милевски. Дата публикации: 6.2.2019
Магнитно-резонансная томография (МРТ) в Санкт-Петербурге
Запишитесь на МРТ по телефону (812) 493-39-22 или заполните форму
Расписание приема МРТ:
ЦМРТ «Нарвский»
(812) 493-39-22
в четверг прием с 8-00 до 23-00
и воскресенье прием с 8-00 до 23-00
ул. Ивана Черных,29
МРТ аппарат 1,5 Тл
суббота :
ЦМРТ «Старая деревня»
(812) 493-39-22
прием 8-00 до 23-00
ул. Дибуновская,45
МРТ аппарат 1,5 Тл
Прием в “РНХИ им. проф. А.Л. Поленова” прекращен по техническим причинам и
перенесен в ЦМРТ
Лучевая диагностика поражений вилочковой железы
ЛУЧЕВАЯ ДИАГНОСТИКА ПОРАЖЕНИЙ ВИЛОЧКОВОЙ ЖЕЛЕЗЫ ПРИ МИАСТЕНИИ
По материалам главы из монографии «Миастения» под ред.проф.С.В.Лобзина
Лучевая диагностика и лечение миастении при опухолевом и неопухолевом поражении вилочковой железы (ВЖ) до настоящего времени представляют серьезную проблему. Учитывая прямую связь миастении с патологическими изменениями ВЖ, выявление миастенических расстройств должно служить косвенным признаком наличия изменений тимуса и являться показаниями к тщательному обследованию органов средостения.
Несмотря на широкое применение различных специальных методов диагностики, ошибки в выявлении новообразований ВЖ превышают 10-20%, что в свою очередь снижает возможности своевременного хирургического лечения. Вопросы диагностики характера поражения вилочковой железы весьма актуальны. Если при опухолевом поражении тимуса показания к операции приближаются практически к абсолютным и выполняются по онкологическим показаниям, то при неопухолевом поражении определенной группе пациентов операция не показана или целесообразна консервативная терапия.
Поражения вилочковой железы разнообразны по своему составу. У больных с миастенией наиболее часто встречается лимфоидная гиперплазия тимуса или тимома.
Тимомы относятся к наиболее частым новообразованиям средостения. Они одинаково часто встречаются у мужчин и женщин, составляют
3–7 % онкологических заболеваний и 10–25 % первичных новообразований средостения. Возраст заболевших в основном от 40 до 60 лет. В 65–70 % наблюдений тимома инкапсулирована, у 30–35 % больных отмечается инвазивный рост, причем наиболее характерно прорастание опухоли в прилежащую плевру или перикард. Отдаленные метастазы встречаются менее чем в 5 % наблюдений.
Разделение тимом на доброкачественные и злокачественные в определенной степени условно, а гистологическая характеристика для этого нередко является недостаточной. Ряд авторов считают, что отличия между доброкачественными и злокачественными тимомами не столько
морфологические, сколько клинические, и предлагают тимомы называть не злокачественными, а «инвазивными» или «метастазирующими».
Основным признаком злокачественной тимомы, кроме метастазирования, является наличие инвазии в органы и ткани грудной полости, т.е. выход за пределы капсулы опухоли. При отсутствии инфильтративного роста тимому следует считать доброкачественной, что, однако, не исключает возможности рецидивов опухоли. Опухоли с выраженной атипией эпителиальных клеток и инвазивным ростом расцениваются как рак вилочковой железы.
К настоящему времени принята классификация тимом, предложенная экспертами ВОЗ, под редакцией J. Rosai в 1999 г. и модифицированная
в 2004 г. В ней выделяют следующие типы тимом:
Тип А – веретеноклеточная; медуллярная;
Тип В1 – богатая лимфоцитами; лимфоцитарная; преимущественно кортикальная; органоидная;
Тип В2 – кортикальная;
Тип В3 – эпителиальная; атипичная; сквамоидная; высокодифференцированный рак тимуса;
Тимомы типа А (медуллярноклеточные, темноклеточные или веретеноклеточные) составляют не более 5 % всех тимом, расцениваются как
доброкачественные и, за редким исключением гормонально-неактивные.
Тимомы типа АВ (смешанные, медуллярно- или темноклеточные с умеренным количеством лимфоцитов) составляют около 10 % тимом,
чаще доброкачественные и гормональнонеактивные. По клиническим проявлениям они неотличимы от тимом типа А.
Тимомы типа В (В1, В2, В3) составляют до 70–80 % тимом и представляют наиболее неоднородную группу, особенно в плане прогноза. Мультицентричный рост наблюдается у 20–30 %, а инвазивный – у 50 % больных. Для них характерны сдавление и прорастание органов средостения, паранеопластические аутоиммунные заболевания.
Рак тимуса – редкая опухоль (менее 5 % новообразований тимуса), отличается быстрым инвазивным характером роста и ранним проявлением имплантационных (по плевре и перикарду), лимфо- и гематогенных (в легких, печени, костях, реже в надпочечниках, головном мозгу) метастазов.
Для уточнения показаний к тимэктомии исключительно важное значение имеет лучевые методы исследования, позволяющие установить характер эволюции вилочковой железы (инволюция, гиперплазия, опухоль).
Первое обстоятельное описание рентгенологической картины новообразований вилочковой железы принадлежит Lenk (1929). Изучение основывалось на данных рентгеноскопии и рентгенографии органов грудной клетки. Отсутствие современных методов исследования было основной причиной того, что картина представленная этим известным ученым затем приведенная во многих отечественных и зарубежных руководствах, оказалась неточной. Количество ошибок при диагностике новообразований вилочковой железы в 50-е годы достигало 40%, в 60-е – 30%, в 70-е – 25%.
В дальнейшем предпринимались многочисленные попытки улучшить рентгенологическую диагностику заболеваний вилочковой железы. Большой вклад в улучшение визуализации вилочковой железы внесли методики пневмомедиастинографии, пневмомедиастинотомографии, ангиографические исследования сосудов средостения, в том числе, селективная флебография тимуса. Однако, уверенная диагностика структурных изменений вилочковой железы, стала возможна только с появлением цифровых компьютерных технологий. Из рентгенологических методов к ним относится мультиспиральная компьютерная томография.
Компьютерная томография
Изучение отечественных и зарубежных работ, посвященных методам диагностики генерализованной миастении, позволяют заключить, что установление диагноза “миастения” требует безотлагательного исследования состояния ВЖ особенно у больных в возрасте старше 30 лет. Следует уделять особое внимание тщательному радиологическому обследованию переднего средостения у пациентов с началом генерализованной миастении (ГМ) после 40–45 лет, поскольку именно у таких больных сочетание миастении и тимомы отмечается наиболее часто (40–70%).
Патологические изменения в ВЖ, согласно данным литературы, при миастении наблюдают у 90–100% больных.Анализ литературы не оставляет сомнений, что МСКТ является необходимым и часто достаточным
методом для исследования области ВЖ. А с учетом преимущественно бессимптомного течения тимом, лучевые методы играют ведущую роль в их обнаружении. При этом, по мнению ряда авторов, тимомы являются наиболее частыми образованиями средостения, диагностированными на начальной стадии при помощи МСКТ.
Высказывается мнение, что присоединение ГМ у больных с тимомами в некоторой степени благоприятствует успешному и своевременному лечению опухолевого процесса благодаря более раннему радиологическому исследованию переднего средостения. Более того, в ряде работ показано, что наличие ГМ является независимым прогностическим фактором, обусловливающим более благоприятный исход у пациентов с тимомой.
Известно, что с периода полового созревания до, приблизительно, 25-летнего возраста, ВЖ выглядит как четко очерченная треугольная или двудольчатая структура, окруженная медиастинальной жировой клетчаткой.
В типичных случаях ее границы плоские или слегка вогнутые по бокам. Границы также могут быть выпуклыми, что более характерно для
детского возраста. После 25 лет ВЖ при КТ средостения визуализируется в виде мягкотканных островков на фоне наличия выраженной жировой клетчатки. Скорость и степень инволюции железы варьируют у разных людей, поэтому тимус может определяться как отдельная структура до 40 лет. Информативность метода КТ в определении объемных образований ВЖ может снижаться за счет существенных изменений, которые развиваются в ткани тимуса с возрастом и значительных вариаций в размерах и весе ВЖ, в частности, у людей в возрасте 25–40 лет, когда железа может быть выражена и затрудняет диагностику тимом. В то же время у больных старше 50 лет обнаружить тимому легче, поскольку железа замещена жировой тканью. Однако ошибки при интерпретации данных КТ случаются во всех возрастных категориях. Гиперплазия ВЖ часто присутствует у пациентов моложе 25 лет, но из за высокой плотности паренхимы может быть скрытой. Изучение вариантов строения вилочковой железы на компьютерно-томографических изображениях позволяет уверенно диагностировать патологические процессы в ней.
Нормальная КТ-анатомия вилочковой железы
Тимус расположен в верхней части грудной клетки, непосредственно за грудиной (верхний отдел переднего средостения). Спереди к нему прилежит рукоятка и тело грудины до уровня IV реберного хряща; сзади — верхняя часть перикарда, покрывающего начальные отделы аорты и легочного ствола, дуга аорты, левая плечеголовная вена; с боков — медиастинальная плевра.
Считается, что наиболее часто тимус на аксиальных срезах ри компьютерной томографии имеет треугольную или двудольчатую форму.
Наиболее важным размером является толщина доли. У пациентов до 20 лет она не должна превышать 1,8-2,0см, старше 20 лет – толщина доли не более 13мм.
При визуализации тимуса на компьютерных томограммах анализируют структуру ткани железы с помощью денситометрических измерений.
При проведении компьютерной томографии оценивают наличие вилочковой железы и положение в средостении: уровень и отношение к срединной линии, ее форму, линейные размеры, однородность структуры, четкость контуров, измеряют плотность нативно, а также в артериальную, венозную и отсроченную стадии. Аксиальные изображения КТ и комбинированные мультиплоскостные реконструкции могут быть использованы, чтобы идентифицировать инвазию опухоли в крупные кровеносные сосуды, перикард и легочную ткань. Если, опухоль имеет гладкие, четкие границы, однородную плотность, отсутствуют некрозы или кистозные изменения, видна жировая прослойка между опухолью и смежными структурами новообразование можно считать неинвазивным. Если, опухолевое новообразование имеет дольчатую или неправильную форму, нечеткие контуры, неоднородное усиление после внутривенного контрастирования, явное прорастание перикарда, легочной ткани, грудной стенки такую опухоль необходимо считать инвазивной.
При гиперплазии вилочковой железы форма железы не изменена, может быть двудольчатой или состоять из отдельных участков тимической ткани. Контур тимуса выпуклый, увеличена толщина. После контрастного усиления в отсроченную фазу отчетливо видна однородно накапливающая контраст гиперплазированная ткань тимуса.
Дифференциальная диагностика между гиперплазией и тимомой (рис.3-7) небольших размеров заключается в выявлении новообразования, локально выходящего за контур железы накапливающего контрастное вещество в разные фазы контрастирования отлично от неопухолевой ткани вилочковой железы.
Магнитно-резонансная томография в диагностике поражений вилочковой железы
Применение магнитно-резонансной томографии (МРТ) для исследования структур грудной клетки открыло новые перспективы в прижизненной диагностике многих заболеваний.
Пульсация сердца смещает средостение во время получения изображения, что снижает ценность МРТ. Поэтому синхронизация изображения с сердечным циклом улучшает визуализацию сердца и средостения.
Сосудистые структуры средостения хорошо визуализируются на МР-томограммах ввиду того, что сигнал от просвета сосудов практически отсутствует. Вилочковая железа внутри периваскулярного пространства легче выявляется на МР-томограммах, чем при КТ. Форма, размер, интенсивность сигнала зависит от возраста. У детей вилочковая железа имеет промежуточную интенсивность сигнала, равную интенсивности сигнала от мышц или лимфоузлов. У взрослых интенсивность сигнала от вилочковой железы выше вследствие жировой инволюции, хотя она у разных людей варьирует. Размеры железы у пациентов старше 30 лет, выявленные при МРТ, лучше коррелируют с операционными находками, чем выявленные при КТ. Это связано с лучшей визуализацией инволютивных изменений при МРТ. Хотя вилочковая железа обычно располагается кпереди от крупных сосудов, она может располагаться и ретровазально. Определение локализации вилочковой железы важно для выявления связи аберрантной железы с переднемедиастинальной тимусной тканью но идентификации интенсивности сигнала.
Естественной контрастности МР-томограмм как правило достаточно для получения необходимой диагностической информации. В отдельных случаях для повышения чувствительности и специфичности метода необходимо дополнительное контрастирование. Исследование внутренних органов, в том числе средостения, основываются на быстрой диффузии парамагнетиков из сосудистого русла в опухолевом очаге. В некротических очагах, где нет кровотока, усиление не наблюдается.
Получение хорошего изображения на МРТ вилочковой железы затрудняется дыхательными движениями. Современный подход к визуализации вилочковой железы предполагает исследование на задержанном дыхании. Контрастирование лучше позволяет дифференцировать солидную и кистозную опухоли. Это связано с тем, что кистозный компонент может содержать примеси белка и крови, искажающие сигнал как на Т1-зависимых, так и на Т2-зависимых изображениях. Полное отсутствие контрастирования доказывает мягкотканную природу образования.
Вилочковая железа на МР-изображениях
Форма и сигнал от вилочковой железы меняются с возрастом. Максимальный вес приходится на 12-19 лет, а затем начинается инволюция, представляющая собой замещение ее жировой тканью. Этот процесс отражается на МРТ, особенно, Т1-зависимых.
Нормальная ткань вилочковой железы достаточно хорошо узнаваема на стандартных МРТ по характерной форме, размеру и расположению. Критерии нормальной вилочковой железы включают отсутствие округлых мягкотканых образований > 7 мм; отсутствие выпуклого контура железы у лиц старше 19 лет, отсутствие дольчатости, отсутствие утолщения вилочковой железы (должен быть ≤ 1,3 см после возраста 20 лет)
Однако у подростков и в молодом возрасте она очень вариабельна по размерам и форме, кроме того, плотность ее на КТ и сигнал на МРТ могут быть схожими с опухолевыми поражениями, так как вилочковая железа еще полностью не заместилась жировой тканью. Следовательно, в некоторых случаях дифференциальная диагностика нормальной и опухолевой ткани может представлять сложности.
При гиперплазии отмечается повышение сигнала на противофазных изображениях с возвращением к норме после лечения.
Округлые, инкапсулированные и с четкими краями опухоли вилочковой железы обычно доброкачественные (тип А). Злокачественные варианты имеют неровный контур, кистозные и некротические компоненты, кальцинаты, а также сопровождаются лимфоаденопатией.
МР-заключение о наличии опухоли вилочковой железы обычно базируется на локальном увеличении железы, выявлении связи опухоли переднего средостения с железой. Интенсивность сигнала от опухоли чаще выше, чем от нормальной ткани железы. Большинство инкапсулированных опухолей дают гомогенный сигнал как на Т1, так и на Т2-изображениях. Инвазивные опухоли чаще негомогенные на Т2-зависимых изображениях.
Хорошая визуализация сосудов при МРТ с синхронизацией позволяет выявлять нечеткость их контуров при инвазии опухолью. Перикард на ЭКГ-синхронизированных изображениях выглядит как тонкая линия, низкой интенсивности толщиной менее 4 мм. При его инвазии возможно выявление прерывистости этой линии с замещением ее высокоинтенсивной опухолевой массой.
Кисты вилочковой железы обладают низкой интенсивностью сигнала на T1-зависимых изображениях и высокой на Т2-зависимых. Спонтанное кровотечение в кисту приводит к повышению сигнала на Т1-зависимых изображениях в связи с парамагнитным эффектом метгемоглобина.
Тимолипомы на Т1-зависимых изображениях выглядят как массы с высокой интенсивностью сигнала, что является отражением их жировой природы. Линейные полосы низкой интенсивности сигнала представлены резидуальной фиброзной стромой или тканью вилочковой железы, проходящей через тимолипому.
Фибромы вилочковой железы распознаются довольно легко, так как они дают низкую интенсивность сигнала как на Т1-, так и на Т2-зависимых изображениях.
От правильного выбора тех или иных методов исследования в каждом конкретном случае часто зависит успех лучевой диагностики. Поскольку количество этих методов достаточно велико (рентгенодиагностика, КТ, МРТ, УЗИ, ПЭТ-КТ) в практической деятельности необходимо руководствоваться принципом получения максимума информации при использовании минимума диагностических средств. Этот принцип предполагает использование того метода, который дает наибольший диагностический эффект в наиболее короткий срок.
МРТ СПб технически позволяет выполнять МРТ средостения, однако эта задача стоит редко и предпочтение отдается КТ. Исследование средостения при МРТ в СПб мы проводим как исключение, так как методика исследования требует кардиосинхронизации. Использован наш опыт ГМПБ №2, и работы на аппарате с открытым МРТ.

